ニプロが再生医療等製品「ステミラック注」を本承認申請 「条件及び期限付承認」の期間中に有効性や安全性を検証
更新日:
 イチオシスト
イチオシスト
ライター / 編集
イチオシ編集部 旬ニュース担当
注目の旬ニュースを編集部員が発信!「イチオシ」は株式会社オールアバウトが株式会社NTTドコモと共同で開設したレコメンドサイト。毎日トレンド情報をお届けしています。
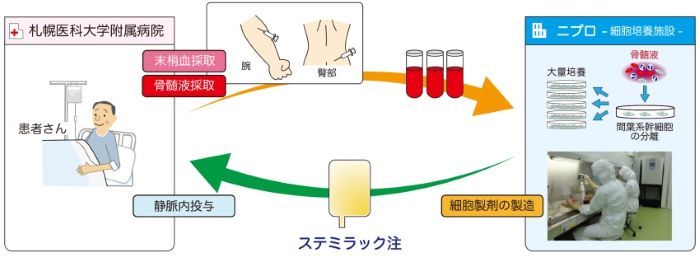
医療機器メーカーのニプロ(大阪府摂津市)は、札幌医科大学(札幌市)と共同開発を進めていた再生医療等製品「ステミラック注」について、厚生労働省に新再生医療等製品の本承認申請を行った、と発表した。
「ステミラック注」は脊髄損傷治療薬で、「脊髄損傷に伴う神経症候及び機能障害の改善を効能、効果又は性能」として、2018年12月28日付で「条件及び期限付承認」を取得していた。
同社は承認期限である7年のうちに、「ステミラック注」を使用した人としない人の比較調査をし、有効性や安全性を社内で検証して本承認申請を行った、としている。
記事提供元:オーヴォ(OvO)
※記事内容は執筆時点のものです。最新の内容をご確認ください。
